Siud: Novo Sistema de Identificação Única de Dispositivos Médicos Entra em Operação no Brasil
3/14/20264 min ler

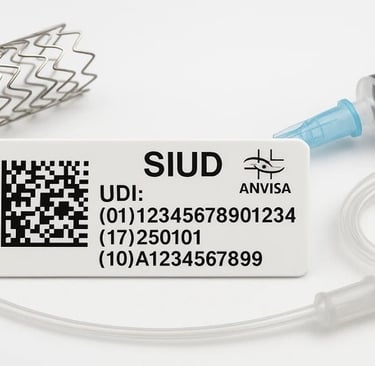
Um Novo Marco para a Rastreabilidade de Dispositivos Médicos
O sistema regulatório brasileiro de dispositivos médicos acaba de dar um passo importante para fortalecer a segurança sanitária e a rastreabilidade de produtos utilizados em procedimentos de saúde.
A Agência Nacional de Vigilância Sanitária iniciou a operação do Sistema de Identificação Única de Dispositivos Médicos (Siud), uma plataforma que permitirá maior controle e transparência sobre a cadeia de produção e distribuição desses produtos no país.
A implementação do sistema está alinhada às melhores práticas regulatórias internacionais definidas pelo International Medical Device Regulators Forum, fórum global de reguladores de dispositivos médicos do qual o Brasil é membro.
A iniciativa cumpre o que foi estabelecido pela Instrução Normativa nº 426/2026 e pela RDC nº 591/2021, que definiram os requisitos para transmissão e gestão da base de dados sobre Identificação Única de Dispositivos Médicos (UDI) no Brasil.
Neste blog, você entenderá como funciona o Siud, quais são os impactos para empresas do setor e como se preparar para as novas exigências regulatórias.
Índice
O que é o Sistema de Identificação Única de Dispositivos Médicos (Siud)
Como funcionará a implementação do sistema
Informações importantes para empresas do setor
Benefícios da identificação única de dispositivos médicos
Impactos regulatórios para fabricantes e importadores
Como a DSL CONSULT pode ajudar
O que é o Sistema de Identificação Única de Dispositivos Médicos (Siud)
O Siud é uma plataforma criada para gerenciar a base de dados da Identificação Única de Dispositivos Médicos (UDI) no Brasil.
Esse sistema permite que cada modelo de dispositivo médico tenha um código de identificação único, associado a informações detalhadas sobre o produto, seu fabricante e sua cadeia de distribuição.
Com essa identificação padronizada, será possível:
rastrear dispositivos médicos ao longo de toda a cadeia produtiva
monitorar a circulação de produtos no mercado
facilitar ações de vigilância sanitária e recall
ampliar a transparência das informações sobre os dispositivos
Esse modelo de rastreabilidade já é utilizado em diversos mercados regulatórios internacionais.
Como funcionará a implementação do sistema
A transmissão de dados ao Siud já está disponível de forma voluntária para as empresas do setor.
No entanto, a obrigatoriedade será implementada de forma gradual, seguindo os prazos estabelecidos pela RDC nº 591/2021.
Essa implementação progressiva permitirá que fabricantes, importadores e detentores de registro adaptem seus sistemas internos e seus processos regulatórios para atender às novas exigências.
Informações importantes para empresas do setor
Para apoiar o setor regulado durante a implementação do sistema, a Anvisa disponibilizou diferentes recursos e orientações.
Entre eles estão:
Lista de dispositivos com transmissão suspensa
A agência publicou uma lista de dispositivos médicos com transmissão suspensa ao Siud, ou seja, produtos temporariamente bloqueados para envio de dados.
Essa medida está prevista no artigo 13 da Instrução Normativa nº 426/2026.
Manuais e orientações do sistema
Também estão disponíveis no portal da Anvisa manuais e instruções detalhadas sobre o funcionamento do sistema, incluindo orientações para envio e gestão dos dados.
Esses materiais foram disponibilizados ao setor regulado desde 2025, com o objetivo de facilitar a adaptação das empresas às novas exigências.
Benefícios da identificação única de dispositivos médicos
A implementação do sistema de identificação única traz avanços importantes para o setor de saúde no Brasil.
Entre os principais benefícios estão:
Rastreabilidade
O sistema permitirá acompanhar todo o percurso de cada dispositivo médico, desde sua fabricação até a utilização pelo paciente.
Transparência
As informações sobre dispositivos médicos se tornam mais claras e acessíveis para profissionais de saúde, empresas e cidadãos.
Segurança
Com mais dados disponíveis sobre os produtos, torna-se possível identificar riscos com mais rapidez e adotar medidas de proteção à saúde pública.
Impactos regulatórios para fabricantes e importadores
A implementação do Siud representa uma mudança relevante para empresas que atuam com dispositivos médicos.
Entre os principais impactos estão:
necessidade de estruturação da identificação UDI dos produtos
adequação dos sistemas internos de gestão de dados
integração com a base de dados regulatória da Anvisa
atualização de processos de rastreabilidade e monitoramento pós-mercado
Empresas que se anteciparem a essas mudanças tendem a enfrentar menos dificuldades na adaptação às exigências regulatórias futuras.
Como a DSL CONSULT pode ajudar
A implementação de novos sistemas regulatórios, como o Siud, reforça a importância de uma estrutura regulatória sólida para empresas que atuam com dispositivos médicos.
A DSL CONSULT atua no suporte técnico e estratégico para empresas do setor da saúde que precisam estruturar ou manter a conformidade regulatória de seus produtos junto à Anvisa.
Entre os principais serviços oferecidos estão:
· estruturação de processos de regularização de dispositivos médicos
· organização de dossiês técnicos e documentação regulatória
· suporte em registros, notificações e alterações pós-registro
· orientação sobre requisitos regulatórios aplicáveis ao produto
· acompanhamento de processos regulatórios junto à Anvisa
Com foco em segurança regulatória, governança documental e sustentabilidade operacional, a DSL CONSULT auxilia empresas a manterem seus produtos alinhados às exigências sanitárias e às constantes atualizações regulatórias do setor.
Conclusão: Um Novo Nível de Segurança para Dispositivos Médicos
A entrada em operação do Siud representa um avanço importante para o sistema regulatório brasileiro.
Com maior rastreabilidade, transparência e controle sobre dispositivos médicos, o país se aproxima das melhores práticas internacionais de vigilância sanitária.
Para as empresas do setor, adaptar-se a essas mudanças será fundamental para garantir a continuidade de suas operações e manter a conformidade regulatória.
Se sua empresa precisa se preparar para as exigências relacionadas à identificação única de dispositivos médicos, conte com o suporte especializado da DSL CONSULT para estruturar o processo regulatório anterior ao Siud.
Endereço
Parque Tecnológico - Univap
Av. Shishima Hifumi 2911 . Sl 302 . São José dos Campos . SP
→ (12) 99634 -7107
→ (12) 98825 -6227
→ (12) 99102 -7272
contato@dslconsult.com.br
comercial@dslconsult.com.br


Contato
Serviços
Consultoria ANVISA
Projetos Arquitetônicos
Licença Sanitária (LS)
Autorização de Funcionamento (AFE/AE)
Certificação Boas Práticas de fabricação/Distribuição
Certificação INMETRO
Notificações e Registros ANVISA
Treinamentos e auditorias
Hospedagem de de equipamentos
Venda de Empresas com Autorização de Funcionamento (AFE)
